Tartalom
Az atomok a legkisebb részecskék, amelyek még mindig megtartják egy elem kémiai tulajdonságait. Ezek szubatomi részecskékből állnak, úgynevezett neutronok, elektronok és protonok. Az ionok töltött atomok vagy atomcsoportok. Az ionok pozitív vagy negatív töltésűek lehetnek. A pozitív töltésű ionokat kationoknak nevezzük. A negatív töltésű ionokat anionoknak nevezzük.
Az atomok alkotóelemeket képeznek a meglévő protonok száma alapján. Az ionos töltések az ionok elektronszámának alapján vannak kiosztva.
Az Atom
Az elemek olyan atomokból álló alapvető anyagok, amelyeket kémiailag nem lehet megváltoztatni vagy tovább bontani. Az atomok magmagból és orbitális elektronokból állnak. A mag protonokból és neutronokból áll. A protonok olyan kis részecskék, amelyek kissé pozitív töltéssel rendelkeznek. A neutronok nagyjából megegyeznek a protonokkal. Nincs díj. Az elektronok nagyon kicsik, még kisebbek, mint a protonok és a neutronok. Az elektronok töltése kissé negatív. Az atommagban levő protonok száma határozza meg, mely elemet alkotja az atom. A atom körül keringő elektronok, különösen a valencia elektronok száma meghatározza, hogy az atom milyen reaktív.
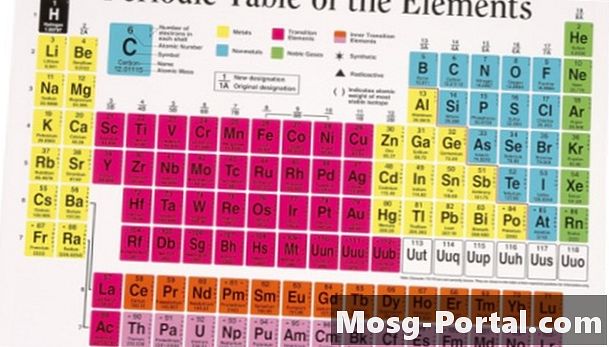
Vegyérték elektronok
Az elektronok egy atommag körül keringnek, mert vonzzák őket a pozitív töltésű protonok. Nem tapadnak a maghoz, mert a többi elektron negatív töltései taszítják őket. Az elektronok hajlamosak keringni rétegeknek nevezett rétegekben. Minden héj „meg van töltve”, ha nyolc elektronból álló oktettet tartalmaz. A legkülső héj a valencia elektronokat tartja. A vegyérték elektronok meghatározzák, hogy az elem milyen reaktív. A különféle elemek atomjai különböző elektronszámúak. Az atom valencia elektronok számát a periódusos táblázat segítségével lehet meghatározni. A periódusos táblában nyolc oszlop található, és az elemek a nyolc oszlop egyikébe vannak rendezve. Az egy elemben lévő valencia-elektronok száma megfelel annak oszlopának, egytől nyolcig terjedően. A nyolcadik oszlopban lévő nemesgázok teljes vegyérték-elektron értékű, és nem túl reakcióképes.
Teljes oktettek
A nemesgázok nagyon stabilak, mert teljes külső héjuk van. A legtöbb elem - a nehézfémek, a lantanidok és az aktinidok kivételével - az oktet szabályt követi. Az oktet szabály szerint az elemek általában olyan reakciókon mennek keresztül, amelyek teljes valenciahéjat eredményeznek. A teljes külső héjú atomok nem nagyon reagálnak, mivel energiiailag stabilak. Az atomok elektronokat cserélnek a stabilitás növelése érdekében.
Elektron transzfer
Ionok képződnek, amikor az atomok elektronokat továbbítanak. Minden atom "azt akarja", hogy a teljes héjában teljes elektron-oktett legyen. A hét valencia elektronú atomok meg akarnak szerezni egy elektronot, hogy összesen nyolc legyen. Az egyik nyerése könnyebb, mint a hét elvesztése. Az egy vegyértékű elektronnal rendelkező atomok el akarnak veszíteni egy elektronot, hogy egy teljes héjra essenek. Az egyik elvesztése könnyebb, mint a hét megszerzése. Az elektronok negatív töltésűek, tehát azok az atomok, amelyek elektronot szereznek az oktettek teljesítéséhez, negatív töltést kapnak és anionokká válnak. Az elektronokat elvesztő atomok negatív töltést veszítenek és kationokká válnak. Az atomok, amelyek több elektronot veszítenek el vagy nyernek, több töltést veszítenek vagy nyernek.