Tartalom
- TL; DR (túl hosszú; nem olvastam)
- Propán osztályozás
- A propán kémiai képlete
- Propán felépítése
- A propán tulajdonságai
- Propán felhasználásai
A propán fosszilis tüzelőanyag és a földgáz egyik alkotóeleme. Több millió év alatt az organizmusok szerves maradványaiból képződött, és a föld alatti lerakódásokból bányozták. A propángáz egy szerves vegyület, amely három szénatommolekulából áll össze, amelyek nyolc hidrogénatommal vannak kötve. A szén-szén-szén-hidrogén kötések típusa határozza meg a propánmolekulák szerkezetét, amely ugyanazt a mintát követi, mint más típusú természetes gázok, például a metán és a bután.
TL; DR (túl hosszú; nem olvastam)
TL; DR (túl hosszú; nem olvastam)
A propán kémiai képlete C3H8.
Propán osztályozás
A propánt szerves vegyületnek kell besorolni, mert széntartalmú. Továbbá szénhidrogén-kategóriába sorolják, mivel az olyan szerves vegyületek csoportjába tartozik, amelyek csak szénből és hidrogénből készülnek. Pontosabban, a propán egy szénhidrogén típusú, alkánnak nevezett szénhidrogén. Az alkán molekulák atomjait egyetlen kovalens kötés tartja össze, és a szénatomok mindig négy kovalens kötést képeznek.
A propán kémiai képlete
Az alkánok egy általános képletet követnek, a szénatomok és a hidrogénatomok meghatározott arányával: C_nH2_n+2. A legegyszerűbb alkán a metán, más néven földgáz. Egy szénatomot tartalmaz, amely négy hidrogénatomhoz kapcsolódik. Metán esetében n = 1, tehát a hidrogénatomok száma 2 (1) +2, ami megegyezik a 4. Az etán két egymással összekötött szénatomot tartalmaz, és mindegyik szén összesen hat hidrogénatomhoz három hidrogénatomhoz kapcsolódik. A propán három szénatomos lánccal rendelkezik, kémiai képlete C3H8, mert három szénláncból 2 (3) +2 hidrogénatomra van szükség, ami nyolc. A butánnak, egy másik szokásos alkánnak, amelyet tüzelőanyagként használnak kézi gázlámpákban, négy szénatomja kapcsolódik tíz hidrogénatomhoz, kémiai képlete C4H10.
Propán felépítése
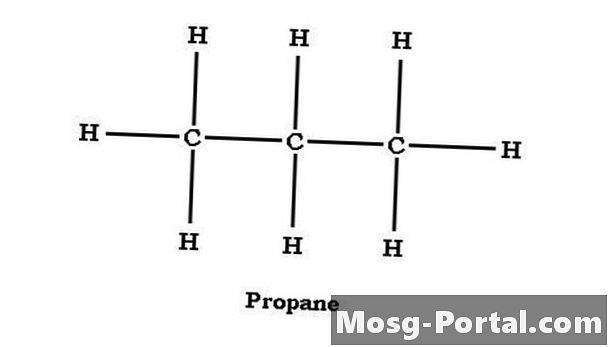
Az alkánok egyenes vagy elágazó láncúak lehetnek. A propán egyenes láncú alkán, a szénatomok strukturált C-C-C. A középső szén egy-egy kötésben van a végső szénatomokkal, és két hidrogénatomot tartalmaz. A végszének mindegyike kötést mutat a központi szénatommal, és mindegyik három hidrogénatommal van kötve. Az egyes szénatomok vonatkozásában a propán CH-ban kifejezhető3CH2CH3, amely megegyezik a C-vel3H8 de világosabbá teszi a propánok szerkezetét.
A propán tulajdonságai
Az egyenes láncú alkánok szerkezeti hasonlóságai mellett hasonló tulajdonságokkal is rendelkeznek. A propán és más szénhidrogének nem polárosak. Ez a tulajdonság azt sugallja, hogy csak más nem poláros anyagokkal keverhetik őket. Például az olajakat és más üzemanyagokat szénhidrogének keverékéből készítik. Nem keverhetők olyan poláris anyaggal, mint például a víz; a molekulák közötti vonzerő elválasztja az olajat és a vizet. Az egyenes láncú alkánoknál a forráspont és az olvadáspont növekszik, amikor a szénmolekulák száma növekszik. A propán forráspontja –44 Fahrenheit fok (–42 Celsius fok), és –306 fok Fahrenheit olvadáspont (–189 Celsius fok). A csak egy szénatomszámú metán alacsonyabb forráspontú, mint a propán, –164 Celsius fokon. Az oktán nyolc szénatomot tartalmaz, forráspontja 98 Celsius fok.
Propán felhasználásai
Alacsony forráspontja miatt a propán általában gáznemű. Amikor a propánt megfelelő mennyiségű nyomáson és hőmérsékleten alkalmazzák, ez egy cseppfolyósításnak nevezett folyamaton megy keresztül, amely a propán gázt folyékony állapotba állítja. A propánt folyadékként tárolhatjuk túlnyomásos tartályokban, jóval forráspontja felett. A cseppfolyósított propángázt fűtőanyagként használják, amelyet égetőkemencékbe és melegvíz-melegítőkbe égetnek el. Főzőüzemként használják kültéri gázrácsokhoz és gáztüzelésű kemping főzőlapokhoz is. A propángáz az aeroszolos kannákban használt hajtóanyagok alkotóeleme is. A propánt alkotóelemként használják bizonyos típusú ragasztókban, tömítőanyagokban és festékekben is.